成大揭開缺氧適應新機制 核酸研究再登國際頂尖期刊
文、圖/成大新聞中心
國立成功大學醫學檢驗生物技術學系陳百昇老師帶領的研究團隊,發現缺氧誘發因子 HIF-1α 除了擔任轉錄因子外,還能在細胞核內「重塑」RNA 代謝路徑,揭示癌細胞在缺氧環境下調節基因表現與能量利用的一種全新適應策略。相關成果刊登於《核酸研究》(Nucleic Acids Research)。A non-canonical role for HIF-1α: redirecting DGCR8 to the RNA exosome for snoRNA degradation and translational modulation. (Nucleic Acids Research, 2026). doi: doi.org/10.1093/nar/gkag070.

成大醫學檢驗生物技術學系陳百昇老師帶領的研究團隊,最新成果再次刊登在國際頂尖期刊《核酸研究》(Nucleic Acids Research)
微核糖核酸(miRNA)等 RNA 生物學相關的重要發現,近年多次獲得諾貝爾獎肯定,讓人類得以進一步探知細胞分子世界裡的奧祕,也對癌症治療等醫學發展帶來重大貢獻。成大醫學檢驗生物技術學系陳百昇老師帶領的研究團隊,繼 2024 年相關核酸研究登上國際頂尖期刊《核酸研究》(Nucleic Acids Research)後,最新研究成果發現缺氧誘發因子 HIF-1α 除擔任轉錄因子外,還可在細胞核內「重塑」RNA 代謝路徑,進而影響核糖體 RNA 修飾與蛋白質生產效率,為理解腫瘤在缺氧與生長刺激下的適應策略提供新視角,近日再度登上該期刊。
人體由數 10 兆個細胞組成,每個細胞內更含有成千上萬種不同的分子。就像細胞之間需要交互作用一樣,細胞內的分子也必須透過即時的動態溝通,來維持細胞的生存優勢。對細胞而言,缺氧是一種壓力,同時也是一種刺激。尤其在實體腫瘤的生長過程中,缺氧環境一旦被癌細胞適應並突破生存瓶頸,疾病的進展往往就變得難以控制。
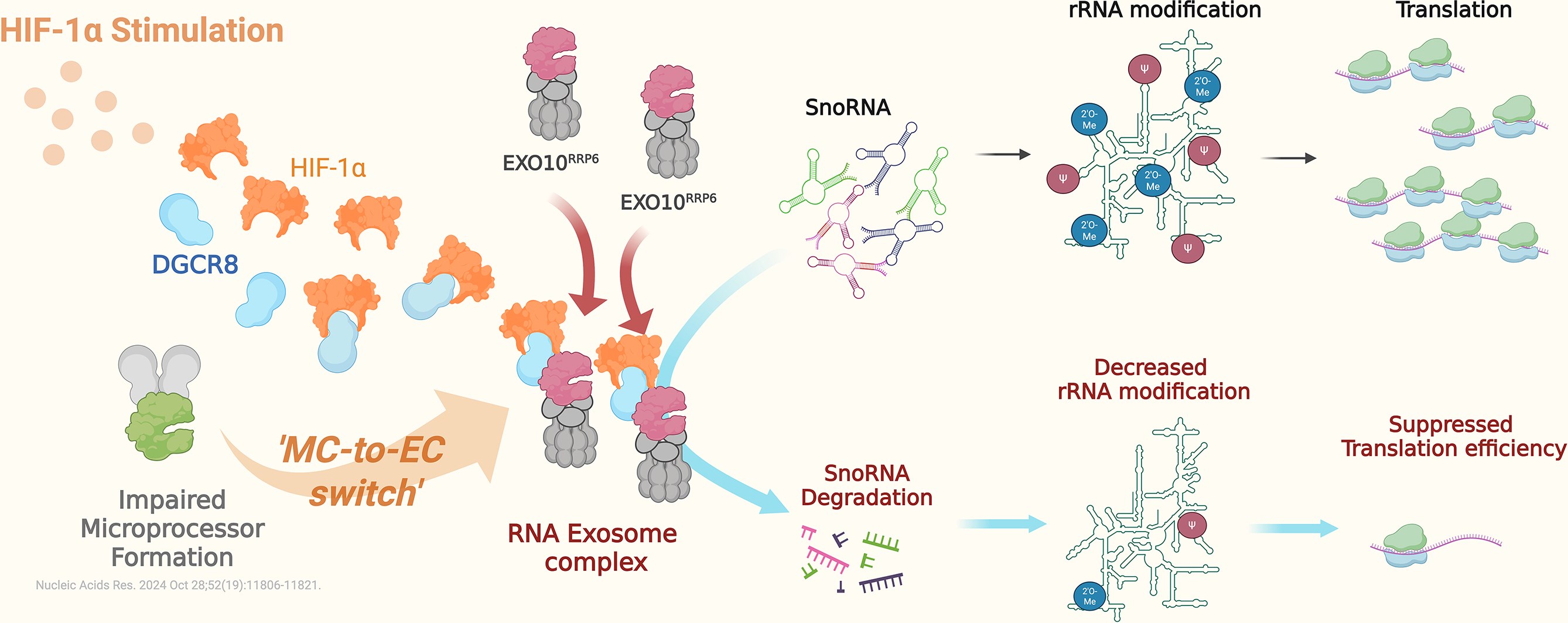
成大醫學檢驗生物技術學系陳百昇老師帶領的研究團隊,最新研究發現缺氧誘發因子 HIF-1α 除擔任轉錄因子外,還可在細胞核內「重塑」RNA 代謝路徑,進而影響核糖體 RNA 修飾與蛋白質生產效率,為理解腫瘤在缺氧與生長刺激下的適應策略提供新視角
該研究的第一作者李婕寧博士後研究員表示,缺氧狀態下的存活壓力,迫使癌細胞演化出一套複雜且精緻的適應機制。首先,缺氧誘發因子(HIF-1α)會大量累積,並啟動下游成百上千個基因,藉此重塑細胞代謝、存活以及血管新生等重要路徑。在此同時,HIF-1α 會阻斷微核糖核酸(miRNA)的生合成,使轉錄後的基因產物(mRNA)得以快速累積而不受抑制。乍看之下,這時細胞內的「蛋白質工廠」似乎應該高速啟動,開始大量生產蛋白質了吧?然而,研究團隊卻發現,HIF-1α 竟然同時伸出另一隻手,啟動 RNA 外切體複合體(RNA exosome complex)的重新組裝,降解了蛋白質工廠中不可或缺的 snoRNA,最終導致整體的蛋白質產線(轉譯作用)受到壓抑。這現象看起來不是很矛盾嗎?
陳百昇表示,這其實一點也不奇怪,反而是癌細胞極為聰明的保護機制。原來,相較於 mRNA 的製造(轉錄),蛋白質的製造(轉譯)在運作時會消耗極大的能量。如果此時無差別地啟動細胞內所有蛋白質的大量產出,細胞將需要耗費數倍甚至數十倍於平常的能量。偏偏缺氧環境通常伴隨著養分的匱乏,這時的能量就顯得無比珍貴。
如果將缺氧視為一場緊急狀況,整體蛋白質生產的降速,就像是高速公路上全面減速讓道的車輛;而應付緊急狀況的「救護車」,則搭載著缺氧誘發的關鍵基因,從路肩超車救急,精準產出應對缺氧所需的蛋白質。透過這套機制,癌細胞得以在逆境中,用最有效率的方式存活下來。原來,癌細胞也深諳《孫子兵法》中「善守者,藏於九地之下」的策略,透過極致的資源管控來度過缺氧危機。

成大醫學檢驗生物技術學系陳百昇老師(左一)帶領的研究團隊,最新成果再次刊登在國際頂尖期刊《核酸研究》(Nucleic Acids Research),圖中右二為第一作者博士後研究員李婕寧
陳百昇團隊一系列的突破性研究成果,從 2018 年發現 HIF-1α 如何以非轉錄方式抑制 Dicer 而促進癌轉移(Journal of Clinical Investigation, 2018),到 2024 年解開 HIF-1α 如何干擾微處理器組裝而影響 miRNA 核內成熟(Nucleic Acids Research, 2024);最新突破則是更進一步破解 HIF-1α 如何把 DGCR8「改派」到 RNA 外切體,透過 snoRNA-rRNA-蛋白質轉譯軸線,協助細胞在缺氧狀態下調節能量支出,為腫瘤如何適應環境壓力提供了關鍵的科學解答(Nucleic Acids Research, 2026)。
至於接下來還有續集嗎?陳百昇笑著表示:「研究沒有終點,這套精密的細胞調控機制也還有許多未解之謎,但面對未知就是一種享受。然而,如果沒有研究資源的挹注,任何科學夢想都只能停留在夢裡,任何困難也只會變成無法跨越的門檻。」因此,研究團隊特別感謝國科會的長期經費挹注,以及來自成功大學、醫學檢驗生物技術學系、醫檢中心、生醫光學影像核心平台、中央研究院、台灣大學,以及美國貝勒醫學院(Baylor College of Medicine)等單位在核心設施及資源上的支持,讓台灣的頂尖研究成果得以持續在國際上受到關注與肯定。
成大表示,《核酸研究》(Nucleic Acids Research)由英國牛津大學出版社(Oxford University Press)出版,為全球核酸領域的頂尖期刊。本研究對未來生物醫學的發展,尤其是疾病機轉以及藥物開發,奠定深厚的科學基礎。
系列研究延伸閱讀:
維護單位:
新聞中心
更新日期:
2026-03-17
瀏覽數:
分享