成大、嘉大團隊破解塑膠微粒擾動腸道菌相之謎 成果登國際頂尖期刊
文、圖/成大新聞中心
塑膠微粒對人體的負面影響近期已被關注到,但因為種類、尺寸複雜,到底對人體有何傷害,還未能釐清,特別是超小尺寸奈米微粒,相關研究更少,成功大學食品安全衛生與風險管理所副教授徐瑋萱與嘉義大學園藝系助理教授李保宏團隊,研究發現奈米微粒竟能「綁架」腸道細胞與細菌的訊息傳遞系統,進一步改變細菌與宿主的共生關係,不僅破壞平衡,更會影響腸道屏障功能,引發腸漏症。這項研究獲得國際高度關注,已發表在頂尖期刊《自然通訊(Nature Communications)》。Polystyrene nanoplastics disrupt the intestinal microenvironment by altering bacteria-host interactions through extracellular vesicle-delivered microRNAs,發表於 Nature Communications

成功大學食品安全衛生與風險管理所副教授徐瑋萱與嘉義大學園藝系助理教授李保宏團隊,研究發現奈米微粒竟能「綁架」腸道細胞與細菌的訊息傳遞系統,進一步改變細菌與宿主的共生關係,不僅破壞平衡,更會影響腸道屏障功能,引發腸漏症。這項研究獲得國際高度關注,已發表在頂尖期刊《自然通訊(Nature Communications)》
團隊利用小鼠進行相關研究,首度揭露奈米塑膠損害腸道健康的新機制,成為塑膠汙染健康風險研究的新里程碑,研究文章在網上發表 3 周,已經有將近 2 萬次閱讀與下載,並獲期刊選為焦點論文(Highlight),社群與大眾媒體的討論熱度 (Altmetric score) ,在全球超過 20 萬篇所有同期文章中名列前 1%,可看出熱門程度。
團隊之前在一項水耕蔬菜研究中,也發現水中的奈米塑膠粒雖未直接傷害萵苣,卻會促進水耕系統中特定細菌的繁殖,這些細菌釋放的外泌體,會抑制作物的抗氧化系統與生長機制,最終導致萵苣枯萎死亡。成果也刊在國際期刊《危險物質(Journal of Hazardous Materials)》。Nanoplastics indirectly compromise lettuce growth in hydroponic systems via microbial extracellular vesicles derived from Curvibacter fontanus,發表於 Journal of Hazardous Materials
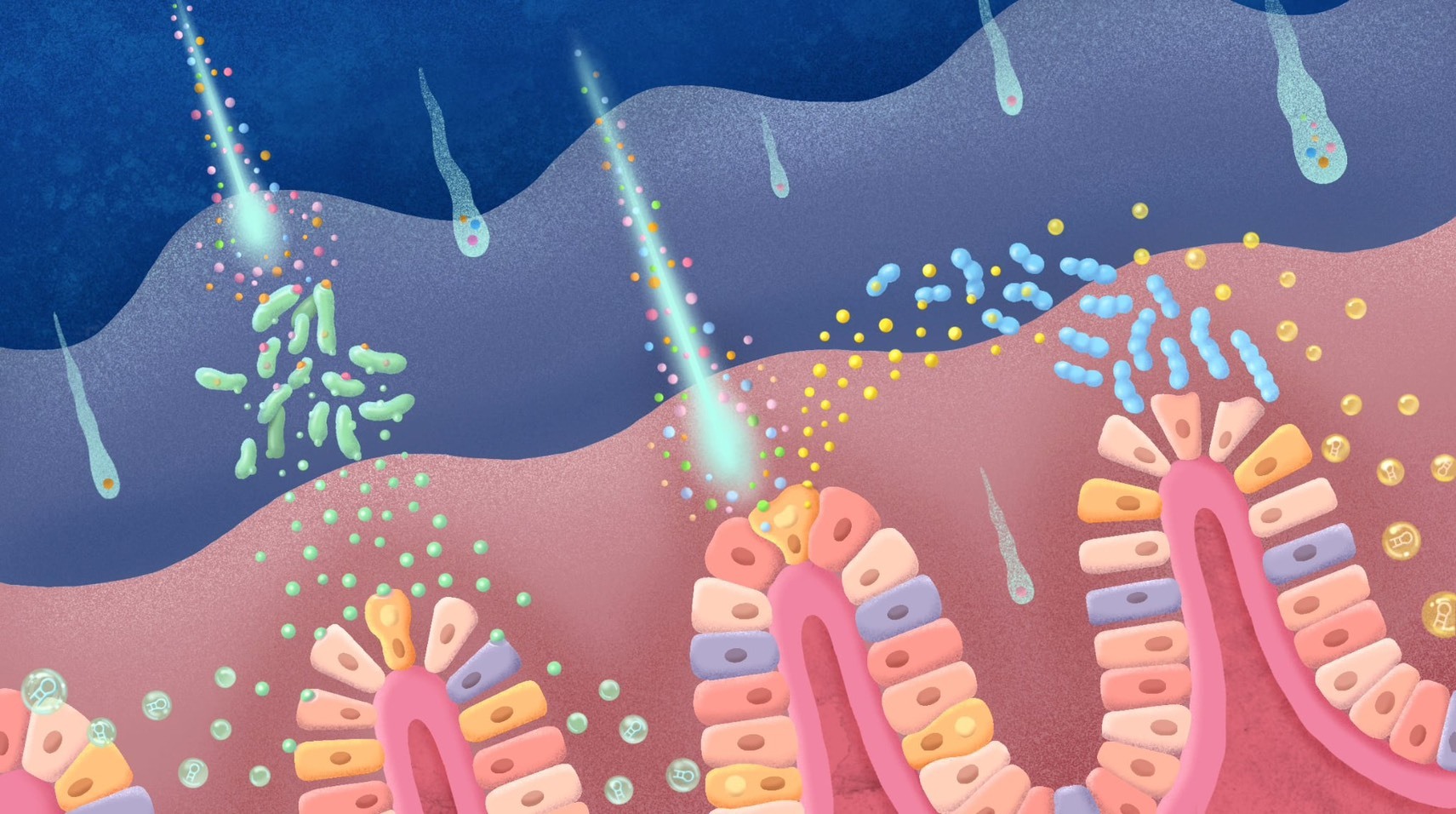
外來的奈米塑膠粒有如彗星穿過腸道保護層,攻擊腸道細菌與腸道細胞。細菌與細胞受到刺激後分泌外泌體,分別影響了腸道細胞間的連結與腸道菌群,造成腸漏現象
徐瑋萱表示,塑膠微粒已成為全球環境的重要隱憂,不只汙染海洋、土壤,現在更證實可能影響作物生長與人體健康。
她表示,塑膠微粒小大不一,過去研究約 150 微米以上的顆粒,進入人體後可能會被排出,但是奈米級的微粒(1 微米等於 1000 奈米)卻可能會堆積在人體各個臟器中,甚至突破腸道與大腦的天然屏障,讓發炎因子或細菌有機會趁虛而入。但因為觀察研究不易,相關的文獻並不多。
團隊指出,「外泌體」是目前科學界重視的研究項目,團隊長期研究外泌體在跨界溝通上的角色(例如動物界與微生物界的溝通),外泌體是一種細胞分泌的微小囊泡,在細胞之間扮演信使,將訊息傳遞給其他細胞,影響其功能。
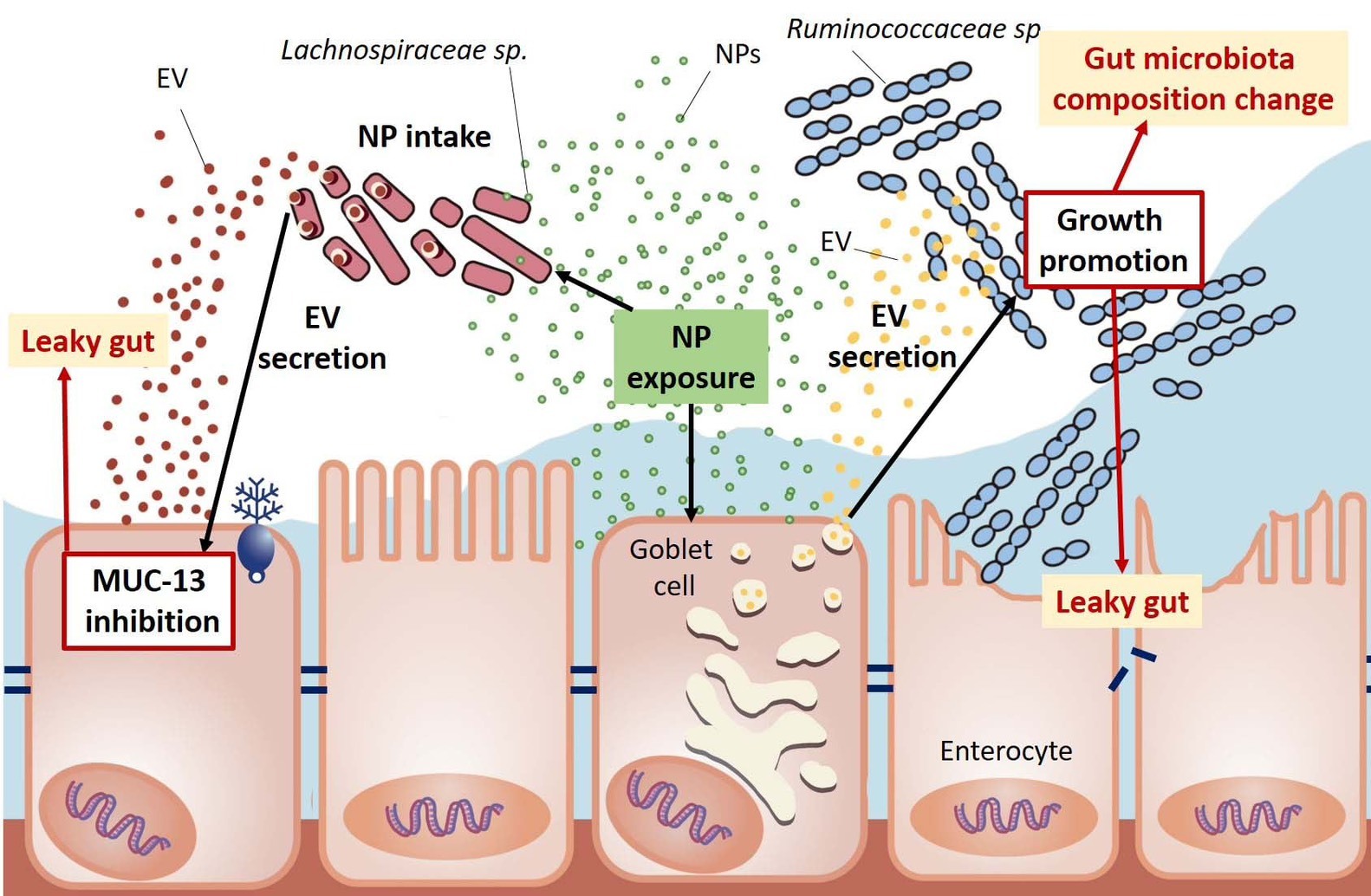
奈米級塑膠粒透過影響腸道細菌與腸道細胞釋放外泌體而破壞腸道菌相平衡與屏障功能
團隊在實驗中餵食小鼠奈米微粒 12 周,發現奈米塑膠透過腸道細胞與腸道特定細菌釋放的外泌體,攜帶的小分子核糖核酸(微小 RNA/microRNA),竟然能夠重新編碼腸道的運作指令,改變細菌與宿主的共生關係,進而引發腸道菌相失衡,好菌減少、壞菌增加,腸道的天然屏障也受隕。團隊表示,這兩項研究首次系統性揭露,奈米粒徑的塑膠微粒可透過影響微生物或宿主細胞的外泌體,間接損害生物體,不論是植物或動物,影響範圍廣泛,潛藏風險不容小覷。
徐瑋萱表示,此研究破解塑膠微粒擾動腸道菌相的分子機制,但因為小鼠與人類的腸道菌相仍存在差異,研究尚無法直接推論對人類的危害,後續仍需進一步評估,團隊已建構人體腸道仿生微生物動態系統,將用於評估奈米塑膠或其它受測物質對人體腸道菌相的影響程度。。而腸道黏膜出現發炎和受損,導致腸道細胞間產生間隙,使原本不應該進入血液的物質,如未完全消化的食物、細菌、毒素等,滲透進入血液循環,進而引發各種健康問題,也就是腸漏症。

成功大學與嘉義大學合作團隊深耕微生物外泌體之功能研究,成果獲 2024 年國科會未來科技獎,圖右 4 為成大食安所副教授徐瑋萱,左 3 為嘉大園藝系助理教授李保宏,與實驗室學生合影
她並表示,研究不僅拓展了對微型塑膠毒性的認知,更突顯外泌體在菌群與宿主間對話中所扮演的核心角色,也為未來療法打開新方向,或許可以透過調控外泌體生成或修復微小 RNA 訊息,來反制奈米塑膠干擾。
李保宏表示,研究關注外泌體在宿主與微生物交互作用的角色,探究外泌體如何調控腸道菌相與宿主健康狀況,為一新穎且極為重要的議題,期待未來以微生物外泌體開發相對應的治療標的。
團隊表示,研究獲國科會「優秀年輕學者計畫」支持及衛福部的經費挹注,能獨立完成這項研究,證明台灣具備堅強的創新能量,目前國際間外泌體相關產品蓬勃發展,研究團隊期許台灣能投入更多資源於外泌體之研究與應用,跟上全球外泌體研究熱潮,建立國際能見度以及取得領先地位。
維護單位:
新聞中心
更新日期:
2025-07-03
瀏覽數:
分享